打一波广告:衢州氟瑞专业生产含氟特种锂电池电解液添加剂
一、锂电池
锂电池是用锂金属或锂合金为作正/负极活性物质、使用非水电解质溶液的化学电池。锂的标准电极电位最负(-3.03V),在金属中比重最轻,反应活泼性最高,因而锂电池的电动势和比能量很高,是一种重要的高能电池。
锂电池结构大致分为五部分,即正极、负极、隔膜、电解液和外壳。
锂电池大致可分为两类:锂金属电池和锂离子电池。锂金属电池以二氧化锰作为正极材料、用金属锂或合金金属作为负极材料,使用时发生放电反应:Li+MnO2 →LiMnO2。一般的锂金属电池是一种一次性电池,无法完成二次充电功能。可充电电池的第五代产品锂金属电池在1996年诞生,其安全性、比容量、自放电率和性能价格比均优于锂离子电池。但由于其自身的高技术要求限制,现在只有少数几个国家的公司在生产这种锂金属电池。
锂离子电池使用锂合金金属氧化物作为正极材料、主要使用石墨作为负极材料。正极材料主要有钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、镍酸锂(LNO)、镍锰酸锂(LiNi0.5Mn1.5O4)、磷酸铁锂(LFP)、三元层状(镍钴锰NCM或镍钴铝三元NCA)、富锂锰基(Li-rich或者OLO)。负极材料多采用石墨,此外也有锂金属负极材料、合金负极材料、锡基负极材料、氧化物负极材料等用于负极。正极反应放电时锂离子嵌入,充电时锂离子脱嵌。负极反应放电时锂离子脱嵌,充电时锂离子嵌入。锂离子电池通过锂离子在正负极间的传递,可以实现二次充放电。以正极材料钴酸锂为例,充电时:LiCoO4 →Li1-xCoO4 + xLi+ + xe-;放电时:Li1-xCoO4 + xLi+ + xe- → LiCoO4。充电时:xLi+ + xe- + 6C → LixC6;放电时:LixC6→xLi+ + xe- + 6C。如下图所示:
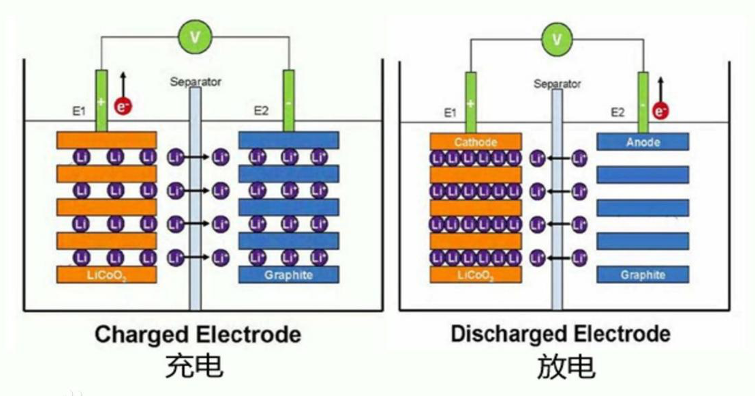
二、非水液态电解质
电解质在锂电池正、负极之间起到传导电子的作用,是锂离子电池获得高电压、高比能等优点的保证。液态电解质一般由高纯度的有机溶剂、电解质锂盐、必要的添加剂等原料,在一定条件下、按一定比例配制而成的。
所采用液体电解质材料一般应当具备如下特性:①电导率高,要求电解液黏度低,锂盐溶解度和电离度高;②Li+导电迁移数高;③稳定性高,要求电解液具备高的闪点、高的分解温度、低的电极反应活性,搁置无副反应、时问长等;④界面稳定,具备较好的正负极材料表面成膜特性,能在前几周期充放电过程中形成稳定的低阻抗固体电解质中间相(solid electrolyte interphase,SEI膜);⑤宽的电化学窗口,能够使电极表面钝化,从而在较宽的电压范围内工作;⑥工作温度范围宽;⑦与正负极材料的浸润性好;⑧不易燃烧;⑨环境友好,无毒或毒性小;⑩较低的成本。
1、溶剂
溶剂起到溶解电解质锂盐,传递锂离子的作用。锂离子电池电解质的性质与溶剂的性质密切相关,一般来说溶剂的选择应该满足如下一些基本要求:①一种有机溶剂应该具有较高的介电常数,从而使其有足够高的溶解锂盐的能力;②有机溶剂应该具有较低的黏度,从而使电解液中Li+更容易迁移;③有机溶剂对电池中的各个组分必须是惰性的,尤其是在电池工作电压范围内必须与正极和负极有良好的兼容性;④有机溶剂或者其混合物必须有较低的熔点和较高的沸点,换言之有比较宽的液程,使电池有比较宽的工作温度范围;⑤有机溶剂必须具有较高的安全性(高闪点)、无毒无害、成本较低。
从溶剂需要具有较高的介电常数出发,可以应用于锂离子电池的有机溶剂应该含有羧基、腈基、磺酰基和醚链等极性基团。对锂离子电池溶剂的研究主要集中在有机醚和有机酯,其中又分环状和链状。
环状醚主要有四氢呋喃、1,3-二氧环戊烷和4-甲基-1,3-二氧环戊烷等。环状醚一般与碳酸二甲酯、碳酸丙烯酯等有机酯溶剂混合使用,因为其在电解液中容易发生开环聚合,不具备稳定的电化学性能,很大程度上限制了其在电解液中的应用。链状醚主要有二甲氧甲烷(DMM)、1,2-二甲氧乙烷(DME)、1,2-甲氧丙烷(DMP)等。一般来说,电解液溶剂的碳链越长,它的耐氧化性能就越强,但同时粘度就越大,电导率也就越低。链状醚能与电解液锂盐六氟磷酸锂(LiPF6)的阳离子反应形成稳定的螯合物,使得锂盐的溶解度增加,从而提高电解液的电导率,但其和锂有较强的反应活性,难以形成稳定的SEI膜。因此,醚类溶剂主要应用于一次性锂电池中。
酯类溶剂主要包括羧酸一元酯和碳酸二元酯两类。环状羧酸酯最重要的是γ-丁内酯(BL)。一般来说,随着碳原子数的增加,环状羧酸酯的介电常数、熔点、粘度会降低,而BL遇水易分解,毒性大,循环效率也远低于碳酸酯有机溶剂,所以这类大分子环状羧酸酯多用于一次性电池中。链状羧酸酯常见的是甲酸甲酯、甲酸乙酯、乙酸乙酯等。链状羧酸酯具有较低的熔点、易于纯化、较高的介电常数等优势,但由于它极性强,比较容易与锂发生反应,不利于电池的循环性能。碳酸酯是目前市场上最常见、最成熟的商业化电解液溶剂。环状碳酸酯最常用的是碳酸乙烯酯(EC)和碳酸丙烯酯(PC)。EC具有较高的热稳定性和介电常数以及较低的粘度,有利于锂盐的溶解和离子的传导,有利于SEI膜的形成,但EC的熔点较高,影响电池的低温性能。PC具有较高的介电常数和化学、电化学稳定性,但PC在负极SEI膜形成之前,容易随着锂嵌入石墨层,使得石墨层发生剥离,导致电池的循环性能下降。链状碳酸酯主要包括碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、碳酸甲乙酯(EMC),它们具有较低的粘度、较低的介电常数。DEC和DMC单独使用不能在锂表面形成稳定的SEI膜,而EMC则热稳定性较差。
单一的溶剂难以满足电解质的各项性能要求,因此实际应用中通常是几种性质不同的有机溶剂混合使用。例如对于有机酯来说,其中大部分环状有机酯具有较宽的液程、较高的介电常数和较高的黏度,而链状的溶剂则具有较窄的液程、较低的介电常数和较低的黏度,所以一般在电解液中会使用链状和环状的有机酯混合物来作为锂离子电池电解液的溶剂。
2、锂盐
锂盐即电解液中锂离子的主要提供者,应用于锂离子电池的锂盐需要满足如下一些基本要求:①在有机溶剂中具有比较高的溶解度,易于解离,从而保证电解液具有比较高的电导率;②具有比较高的抗氧化还原稳定性,与有机溶剂、电极材料和电池部件不发生电化学和热力学反应;⑧锂盐阴离子无毒无害,环境友好;④生产成本较低,易于制备和提纯。
经常研究的锂盐主要是基于温和路易斯酸的一些化合物,这些化合物主要包括磷酸锂(LiPF6)、硼酸锂(LiBF4)、高氯酸锂(LiClO4)、砷酸锂(LiAsF6)、和锑酸锂(LiSbF6)等;以及一些有机锂盐,如LiCF3SO3、LiN(SO2CF3)2及其衍生物。六氟磷酸锂(LiPF6)是目前商品锂离子电池中广泛使用的电解质锂盐,其综合性能最有优势,主要缺陷是高温下不稳定、对水敏感。四氟硼酸锂(LiBF4)有较好的综合性能,其中高低温性能均优于LiPF6,但是它的电导率不高、容易与金属锂发生反应。很多锂盐普遍都具有比较好的综合性能,但都存在个别严重的缺陷,因此限制了它们的大规模应用。
3、电解液添加剂
商品的锂离子电池可能包含10种以上的添加剂,这些添加剂的特点是用量少但是能显著改善电解液某一方面的性能。它们的作用一般有提高电解液的电导率,提高电池的循环效率,增大电池的可逆容量,改善电极的成膜性能,提高电池的安全性等。
1)成膜添加剂
一般负极材料(如碳、硅等)的嵌锂电位低于1.2 V vs. Li+/Li,在锂离子电池首次充电过程中不可避免地要与电解液发生反应,溶剂分子、锂盐或添加剂在一定电位下被还原,产生一些不溶物,从而在负极表面形成一层SEI膜。SEI膜的具体组分非常复杂,并且受电池材料、温度等条件影响而有所不同。它是一层电子绝缘离子导电的膜,能够阻止电解液与负极材料的进一步反应,而不影响Li+的通过。SEI膜的形成对改善电极的性质和提高电极的寿命具有不可忽视的作用。但是,SEI膜的存在会降低电极材料颗粒之间的电子接触,降低首周效率,所以一般不希望SEI膜厚度很大。
正材料表面也可能存在界面膜,具有与负极SEI膜相似的性质,能阻止电解液与电极材料之间的进一步反应,不过其形成机理还存在争议。
成膜添加剂比溶剂更容易在负极上被还原,因此加入到电解液中后,它优先于EC等溶剂而在负极上还原,参与形成SEI膜,并且这样得到的膜的离子通透性好,电子绝缘性好,有利于锂离子在充放电过程中进出负极,但负极上的电子不能接触到溶剂分子,提高了倍率性能并且也提高了存储、低温放电和高温充放电等多方面的性能。
成膜添加剂主要分为无机成膜添加剂(如SO2、CO2、CO等小分子以及卤化锂等)和有机成膜添加剂,如碳酸亚乙烯酯(VC)、亚硫酸丙烯酯(PS)、亚硫酸乙烯酯(ES)等,还包括一些卤代碳酸酯。
2)离子导电添加剂
离子导电添加剂的作用是提高电解液的电导率,对提高电解液导电能力的研究主要着眼于促进导电锂盐的溶解和电离以及防止溶剂共插对电极的破坏。
其按作用类型可分为与阳离子作用型(主要包括一些胺类、分子中含有两个氮原子以上的芳香杂环化合物、冠醚和穴状化合物)、与阴离子作用型(主要是一些阴离子受体化合物,如硼基化合物),以及与电解质离子作用型(中性配体化合物主要是一些富电子基团键合缺电子原子N或B形成的化合物,如氮杂醚类和烷基硼类)。目前常用的导电添加剂有12-冠-4醚、阴离子受体化合物和无机纳米氧化物等。
3)阻燃添加剂
安全性是锂离子电池一直以来最为关注的问题,阻燃添加剂的加入能够在一定程度上提高电解液的安全性。它的主要作用机理是:锂离子电池电解液在受热的情况下会发生自由基引发的链式加速反应,而阻燃添加剂能够捕获自由基,阻断链式反应。
主要种类为有机磷化物、有机氟代化合物、卤代烷基磷酸酯以及离子液体。常用的阻燃添加剂有磷酸三甲酯(TMP)、磷酸三乙酯(TEP)等磷酸酯,二氟乙酸甲酯(MFA)、二氟乙酸乙酯(EFA)等氟代碳酸酯和离子液体等。
4)过充保护添加剂
在锂离子电池过度充电时,会发生一系列的反应。首先是过多的Li+从正极材料中脱出,嵌入负极材料中,可能会导致正极材料结构的坍塌和负极锂枝晶的生成,这主要发生在Li不能完全脱出的正极材料,如LiCoO2、Li1+x(NiCoMn)O2等;其次是电解液组分(主要是溶剂)在正极表面发生不可逆的氧化分解反应,产生气体并释放大量热量,从而导致电池内压增加和温度升高,给电池的安全性带来严重影响。
过充问题可以通过外电路的控制和保护解决,当充电电压达到4.1~4.2V时,电子集成回路控制电压不再上升。除此之外,使用过充保护添加剂也是一种有效的方法。它的基本原理是:添加剂的氧化电位略高于正极脱锂电位,当电池超过工作电压之后,添加剂优先发生反应,造成电池的断路或微短路,从而使电池停止工作并缓慢放热,这个过程不破坏电极材料和电解液。而在正常的工作电压范围内,添加剂不参与电池反应。过充保护添加剂主要包括氧化还原电对、电聚合和气体发生三种类型的添加剂。其中氧化还原电对添加剂最为常用,其原理是:当电压超过电池截止电压时,添加剂在正极表面被氧化,氧化产物扩散到负极表面被还原,还原产物再扩散到正极表面继续被氧化,按照此过程循环进行,直到充电结束。最佳的过充电保护添加剂应该具有4.2~4.3V的截止电压,从而满足锂离子蓄电池大于4V电压的要求。
比较常见的过充保护添加剂有邻位和对位的二甲氧基取代苯、丁基二茂铁和联苯等。
5)控制电解液中酸和水含量的添加剂
因锂和水接触会立即发生激烈反应,所以包括电解质在内的全部材料和零部件均需严格脱水, 并可靠密封。但是,即使是电解液中微量的HF和水分,也会造成LiPF6的分解和电极材料表面的破坏,所以要进一步控制电解液中水分和酸的含量。这类添加剂的作用机理主要是靠与电解液中的酸和水结合来降低它们的含量。
目前常用的控制HF含量的添加剂主要有锂或钙的碳酸盐、氧化铝、氧化镁和氧化钡,它们能够与电解液中微量的HF发生反应,阻止它的影响。但这些物质去除HF的速度较慢,因此很难做到阻止HF对电池性能的破坏。而一些酸酐类化合物虽然能较快地去除HF,但会同时产生破坏电池性能的其它酸性物质。控制水含量的添加剂主要是六甲基二硅烷(HMDS)、烷烃二亚胺等吸水性较强的化合物。
6)改善低温性能的添加剂
低温性能是拓展锂离子电池使用范围的重要因素之一。低温下电解液存在粘度增大,电导率降低,SEI膜的阻抗增大等问题,极大地削弱了电池的能量密度、循环性能。目前常规的电解液成分是以LiPF6为电解质盐,以碳酸乙烯酯(EC)为溶剂基体,再加入混合溶剂(如DMC、DEC、EMC等)。该类电解液具有放电容量高,电导率高,内阻小,充放电速率快,与电极材料相容性较好等优点,但EC的凝固点比较高(36℃),所以低温性能不佳。目前改善电解液的低温性能主要有以下途径:一是通过加入低熔点、低粘度的组分,降低EC的含量,以降低低温下电解液的粘度和共熔点。二是使用低温下仍能保持较小的电荷转移电阻的电解质锂盐。三是添加一些成膜添加剂,优化SEI膜组分,使其在低温下的阻抗降低。
常用的改善高低温性能的添加剂有N,N-二甲基三氟乙酰胺、甲基乙烯碳酸酯(MEC)和氟代碳酸乙烯酯(FEC)等。
7)高电压添加剂
高电压添加剂的使用是改善碳酸酯体系电解液抗氧化性的一种有效手段,这类添加剂主要是正极成膜添加剂,作用机理类似负极成膜添加剂,它的HOMO能量略高于溶剂分子,能够提前在正极表面成膜,从而改善正极材料的表面性能,减少正极材料与电解液的接触以达到抑制电解液分解的目的。
目前,常用的高电压添加剂主要有苯的衍生物(如联苯、三联苯)、杂环化合物(如呋喃、噻吩及其衍生物)、1,4-二氧环乙烯醚和三磷酸六氟异丙基酯等。它们均能有效改善电解液在高电压下的氧化稳定性,在高电压锂离子电池中起着非常重要的作用。
另外,研究发现,溶剂的纯度对电解液的抗氧化性也有重要影响,溶剂纯度的提高能够大幅度提高电解液的抗氧化性。如当EC的纯度从99.91%提高到99.979%时,它的氧化电位从4.87 V提高至5.5 V vs.Li+/Li。
添加剂的种类和作用非常多,除了上文详细描述的这些之外还有很多其它的功能添加剂,例如LiBOB和LiODFB等抑制铝箔腐蚀的添加剂,联苯和邻三联苯等改善正极成膜性能的添加剂,三(2,2,2-三氟乙基)亚磷酸酯(TTFP)等提高LiPF6稳定性的添加剂。实际上,某些添加剂本身就是多功能添加剂,例如,12-冠-4醚加入PC溶剂后,在提高Li+的自身导电性的同时,利用冠状配体在电极表面的亲电作用使得Li+在电极界面与溶剂分子反应的可能性大大降低,冠醚对Li+的优失溶剂化作用抑制了PC分子共插,电极界面SEI膜得到优化,减少了电极首次不可逆容量损失;氟化有机溶剂、卤代磷酸酯加入电解液后,不仅有助于形成优良的SEI膜,同时对电解液具有一定的甚至明显的阻燃作用,能够改善电池多方面的性能。
三、离子液体电解质
离子液体电解质,即室温状态下的熔融盐,完全是由阴阳离子组成。由于阴离子或者阳离子体积较大,阴阳离子之间的相互作用力较弱,电子分布不均匀,阴阳离子在室温下能够自由移动,呈液体状态。相比于锂离子电池,普通有机溶剂离子液体有如下优势:①离子液体的蒸汽压非常低,几乎可以忽略;②离子液体具有较宽的液程,大约300℃;③离子液体不易燃;④具有较高的电导率;⑤化学或电化学稳定性好;⑥对水和空气不敏感;⑦无污染且易回收。
离子液体的种类较多,根据有机阳离子的不同可以分为如下几类:含氮杂环类、季铵盐类和季磷盐类等,其中含氮杂环类又包括咪唑盐类、哌啶盐类和吡啶盐类等。组成离子液体的阴离子种类也比较多,按照阴阳离子随机组合,理论上能够组成千万种离子液体。
但是离子液体电解质也存在诸多问题。首先是大部分离子液体黏度较高,比普通有机溶剂高1~2个数量级,导致电池的倍率性能不好;其次是与正负极材料的兼容性差,材料的脱嵌锂和循环性能在离子液体电解质中很难发挥出来;除此之外,离子液体目前价格较高,限制了其在锂离子电池中大规模应用。
降低离子液体的黏度,提高锂离子在其中的迁移速率,是离子液体电解质能够在
锂离子电池中商业化的前提。目前解决这个问题的途径主要有两种:一是将离子液体与有机溶剂或其他材料共混组成溶剂体系。将离子液体与碳酸酯电解质溶液、聚合物或无机陶瓷混合形成的三类电解质获得了大量研究,并取得了较好的结果,这些新体系的发展有望促进离子液体在电池中获得实际应用。二是调节离子液体的阴阳离子结构。研究发现,使用含有不对称结构的离子液体有助于降低其黏度。
四、凝胶聚合物电解质
凝胶型聚合物电解质通常被定义为:聚合物作为整个电解质的骨架部分,起到力学支撑的作用,其网络结构使得碱金属盐和有机增塑剂形成的电解液能够均匀地分布在网络中,而离子的输运主要发生在包含液体电解质的部分。这类电解质的电导率与碱金属盐的有机溶液相当,在室温下一般可以达到10-3 S/cm以上。常用的凝胶型聚合物电解质基体有:聚丙烯腈(PAN)、聚氧化乙烯(PEO)、聚甲基丙烯酸甲酯(PMMA)、聚偏氟乙烯(PVDF)等。凝胶型聚合物电解质的电导率还与有机溶剂的种类有关,常用到EC、PC、BL等有机溶剂作为增塑剂。
五、高电压电解质
进一步提高锂离子电池的能量密度一直以来都是锂离子电池研究的目标。在现有锂离子电池体系下,提高能量密度主要有两种方式:①使用高电压的正极材料,如尖晶石LiNi0.5Mn1.5O4和橄榄石结构的LiCoPO4;②采用高容量的正极材料,如富锂相正极。这两种电极材料都具有比较高的脱锂电位,普通碳酸酯电解液容易被氧化分解。开发具有更宽电化学窗口的高电压电解液是当前锂离子电池电解质发展的重要方向。目前高电压电解液主要包括以下几种体系。
1、砜基电解液
砜类的磺酰基比碳酸酯中的羰基具有更强的吸电子能力,所以占据分子轨道(HOMO)的能级更低,大部分砜类溶剂的氧化电位都能达到5.5 V (vs.Li+/Li)以上,具有优异的电化学稳定性;而且砜类溶剂本身具有很强的阻燃性。因此砜类溶剂在锂电池中也得到了广泛的研究。基于乙基甲基砜和四甲基砜(TMS)具有比较高的离子电导率和比较宽的电化学窗口,能与LiMn2O4和LiNi0.5Mn1.5O4等高电压正极材料有很好的相容性。但乙基甲基砜(EMS)的熔点比较高(36.5℃),低温性能不是很好。甲氧基乙基甲基砜(MEMS)的熔点比较低(约0℃),基于MEMS的电解液使用LiTFSI作为锂盐,具有比较宽的电化学窗口,但是和石墨负极的相容性不好。
砜类电解质存在的很多问题限制了它的应用:砜类溶剂目前的合成相对比较复杂;其熔点大多高于室温,粘度大;与石墨负极的相容性比较差,不能在石墨负极表面形成稳定的SEI膜;以及与Celgard隔膜的浸润性较差,需要使用价格较高的玻璃纤维隔膜来组装电池。加入成膜添加剂或与碳酸酯溶剂共用可以使部分问题有所改善。
2、氟取代碳酸酯体系电解液
氟取代碳酸酯具有低熔点、高氧化稳定性和不易燃等优势,在高温下循环性能和储存性能都明显提高。很多研究者把它作为锂离子电池电解质添加剂或共溶剂使用。氟代碳酸乙烯酯(FEC)、二氟乙酸乙酯(DFEAc)、二(2,2,2-三氟乙基)碳酸酯(DTFEC)等氟代碳酸酯与常规碳酸酯溶剂组成的电解液,通常具有高电导率、高氧化稳定性、良好的电极相容性等优点,显示出优异的循环性能和安全性能。氟取代碳酸酯有望应用于高电压体系的电解质溶剂,但是它的缺陷是对LiPF6的溶解性较差,需要进一步改善。
3、腈类电解液
腈类溶剂具有较高的闪电、较宽的液程、较高的介电常数和较低的黏度。腈类物质的末端亲核腈基是锂离子配位的主要位点,使得锂盐在腈类溶剂中的溶解度较高,所以腈类电解液通常具有较高的离子电导率。戊二腈和己二腈的氧化电位高达8.3 V vs Li+/Li,是已知的氧化电位最高的溶剂。如戊二腈、己二腈和癸二腈等腈类作为共溶剂与碳酸酯溶剂组成的电解液具有较高的电导率、较低的黏度和较强的抗氧化性,与LiNi0.5Mn1.5O4、Li2NiPO4F等高电压正极材料有良好的兼容性。此外,腈类电解液还具有非常优越的低温性能。但是腈类溶剂与负极的兼容性差,需要使用碳酸酯作为共溶剂或者使用VC和LiBOB等成膜添加剂改善其性能。
联系人:徐经理
手机:+86(0)1815701-8567
电话:+86(0)570780-5618
邮箱:sales@fluorio.com
地址: 浙江省龙游县城南发区龙飞路5号